刘战丛医生的科普号
- 医学科普 经皮经肝胆囊穿刺置管引流术(PTGD)
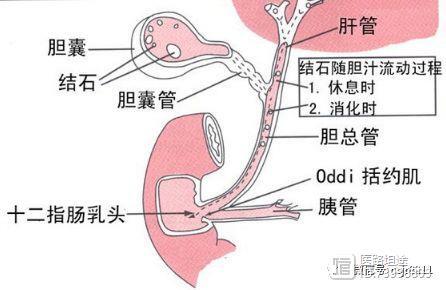
经皮经肝胆囊穿刺置管引流术(PTGD)转自医路坦途2024-02-06发表于河南|1阅读|27转藏经皮经肝穿刺胆囊引流术主要用于治疗急性化脓性胆囊炎、急性重症胆囊炎以及胆总管梗阻合并胆囊肿大者。本术式能够迅速达到胆囊减压的作用,同时还能注入药物,达到治疗目的,尤其适用于老年患者、心肺功能不全患者等不能耐受手术者。一、适应症:1急性胆囊炎,患者症状危重、年老体弱或同时合并严重的心、肺、肝、肾等脏器疾病不能耐受手术者;2胆总管下端梗阻伴胆囊肿大,手术难以切除病灶或解除梗阻,经胆道引流失败者3妊娠期急性胆囊炎;4急性化脓性胆管炎,胆石症并发急性胆管炎的某些病例,肝内胆管扩张不明显而胆囊显著肿大,PTGD比PTBD要简单容易而效果相同;二、禁忌症:1严重出血倾向,出血、凝血机制障碍者2全身衰竭者不能耐受经皮经肝穿刺手术者3陶瓷胆囊或胆囊壁增厚,胆囊壁无法穿刺者4有大量腹水者5胆囊充满结石或无结石而胆囊腔过小者6由于胃肠道气体、肋骨干扰或患者过于肥胖导致胆囊显示不清者7无安全穿刺路径者三、可能并发症拟行超声引导下经皮肝穿刺胆囊置管引流术(PTGD),可能出现:1肝脏出血2胆道损伤3腹腔感染,腹膜炎4胸腔感染,脓胸5胆汁瘘6置管失败7引流管脱落四、技术要点(1)进针深度要求精确,避免进针过浅导致周围组织损伤和引流效果不佳,避免进针过深造成的胆囊后壁及胆囊后方组织的损伤,造成胆汁漏等严重并发症。术前可用测量工具在图像上评估进针的深度,计算针尖进入体内的长度;在术中将图像对比度及增益调至最佳效果,以便实时观测针尖的位置。(2)穿刺时一定要嘱咐患者平稳呼吸。避免呼吸幅度过大导致穿刺针对肝脏造成损伤和因穿刺路径的偏移而导致的穿刺失败。平稳呼吸下匀速进针,到达胆囊床后,嘱患者屏住呼吸,快速进针,刺入胆囊腔内。如果出现一次穿刺置管失败,我们建议终止置管治疗,因为患者胆囊自身张力较大,如果短期内再次置管,有可能会导致胆囊破裂,继发胆汁性腹膜炎。(3)患者的配合程度尤为重要,很多患者可能由于术中疼痛、胆心综合征等导致手术失败,个人体会,术前可以给予止痛及镇静药物联合应用,可以有效减轻患者疼痛及紧张情况,现在提高不能有效配合的患者置管治疗的成功率。五、术后护理:PTGD常见并发症主要是胆汁性腹膜炎、出血、迷走神经反应、小肠瘘、结肠损伤、胆囊或胆道继发感染以及导管脱出等。因此,术后理主要是密切观察引流液的量和性状、保持引流管通畅和防止导管意外脱出。如果发现胆汁混有新鲜出血或引流量突然减少,需及时进行床旁彩超检查,发现问题及时做出相应的处理。PTGD术后引流管的护理尤为重要,术后妥善固定引力管,告知患者,下床活动时将引流袋固定于低于穿刺部位的位置,避免胆汁还流造成逆行感染。术后可以每日应用0.9%生理盐水加庆大霉素8万或甲硝唑250mL每日冲洗两次,冲洗时注意患者反应,冲洗压力适中,避免液体延引流通道进入胆道以外或血管腔内,引起临近器官感染或者脓毒血症。术后2~3周白细胞恢复正常可以试行闭管,当胆囊管通畅时方可拔出引流管。长期置管引流患者,需3月更换一次引流管。总之,PTGD具有微创、安全、费用低廉等优点,掌握其操作方法与注意事项,对提高疗效、改善患者症状、减少术后并发症有积极意义。本文转自医路坦途,致谢!
 刘战丛 主任医师 漯河市中心医院 肝胆胰脾外科8人已读
刘战丛 主任医师 漯河市中心医院 肝胆胰脾外科8人已读 - 医学科普 保胆手术既不能改变胆囊结石的成因,亦不能规避胆囊癌的风险
保胆手术既不能改变胆囊结石的成因,亦不能规避胆囊癌的风险1.“保胆取石”不能祛除结石成因:胆囊结石发病机制仍未明晰,目前认为主要与胆固醇代谢异常、促成核因子作用及胆囊排空功能障碍等多种因素相关。每例患者出现胆囊结石的原因与进程不完全相同,单纯取石不能去除结石成因,术后结石复发率高。有长期随访的临床研究结果显示,保胆取石术后的总体结石复发率为20%~41.5%,随访时间均在1年以上,甚至出现了随访时间越长,复发率越高的趋势[15,16,17,18]。国内少数开展保胆手术的医师同样也进行了临床研究,但普遍存在随访时间短、随访率低、缺少客观结果、统计方法有待改进、不符合循证要求等问题[19,20,21],研究质量不高。另外,目前的药物治疗亦无法避免术后结石复发。2.“保胆取石”无法消除癌变机制:在胆囊结石的病因及疾病发展过程中,胆囊慢性炎症始终贯穿疾病全程,由于慢性炎症会导致局部黏膜DNA损伤,进而活化胆囊的自身修复机制,使得黏膜细胞处于增生的状态,从而加速了“化生-异型增生-癌”这一过程[22];目前无证据表明“保胆取石”能够逆转术后胆囊慢性炎症病程,消除“炎-癌转化”机制;更无法消除胰胆管汇合异常、原发性硬化性胆管炎、慢性肠炎等胆囊癌变因素。3.卫生经济学无获益:“保胆取石”术后由于结石复发率高,多数患者需长期口服熊去氧胆酸等药物。而复发后患者往往需要再次手术,增加了患者的痛苦及医疗费用。4.部分“保胆取石”术后患者的临床症状并未消失:胆囊结石相关的并发症如胆总管结石、胆管炎、胆源性胰腺炎等仍会发生。5.对胆囊腺瘤性息肉行“保胆取息肉”危害极大:保胆取息肉无法去除息肉蒂部,避免息肉复发。而最大径>10mm的腺瘤性息肉已有癌变可能,但多为早期(Tis、T1期),单纯胆囊切除术即可能获得长期生存。对此类患者行“保胆取息肉”术,将不可避免地使含有癌细胞的胆汁外溢至腹腔,极易导致肿瘤腹腔种植转移,危及患者生命。以上内容摘自《胆囊良性疾病外科治疗的专家共识(2021版)》中华外科杂志,2022,60(4) :337-342.DOI:10.3760,致谢!
刘战丛 主任医师 漯河市中心医院 肝胆胰脾外科4人已读 - 图文文章 三阴性乳腺癌精准治疗的机遇
叶青,江泽飞军事医学科学院附属医院乳腺肿瘤科 三阴性乳腺癌(TNBC)是一类有着极大异质性的疾病,个体间生物学行为差异较大,根据基因表达谱分析,TNBC细分为生物学行为各异的6个类别,各类别对不同治疗表现出不同的敏感性。在医疗行业步入精准的时代,寻找TNBC可治疗的各类靶点对不同类别TNBC的精准靶向治疗可能具有指导作用。 乳腺癌已进入分类治疗时代,其中对于芳香化酶抑制剂耐药的激素受体阳性乳腺癌患者,CDK4/6抑制剂、氟维司群等药物提供新的可能,人表皮生长因子受体-2(HER-2)阳性乳腺癌患者的抗HER-2靶向新药不断问世显著改善其预后及生存。三阴性乳腺癌(TNBC)因无治疗性靶点,主要治疗手段仍是化疗。在医疗行业步入精准的时代,如何更加精准治疗TNBC成为研究热点,各类靶向TNBC的新药相继进入临床,为肿瘤患者带来新的希望。本文对TNBC的研究进展和其在精准治疗时代可能的诊疗机遇进行综述。 1 TNBC的分子分型 TNBC是一类异质性的疾病,尽管整体预后不良,但部分患者对化疗敏感,表现出与管腔(Luminal)A型患者相似的良好预后。近年来快速发展的基因组学研究使得再细分这一异质性疾病成为可能。 为更好地定义TNBC特异性分子特征,Lehmann等【1】根据基因表达谱分析将其细分为6个亚型,分别为基底样型1和2(BL1和BL2)、间叶细胞型(M)、间充质干细胞型(MSL)、雄激素受体型(LAR)和免疫调节型(MI)。其中,基底样型TNBC高表达细胞周期和DNA损失相关基因,对顺铂敏感;间叶细胞型和间充质干细胞型的TNBC上皮间质转化(EMT)活跃,表现出对PI3K/mTOR通路抑制剂和达沙替尼(dasatinib)敏感;雄激素受体型的TNBC存在雄激素受体(AR)信号通路和PI3K通路的活化,表现出对AR抑制剂和PIK3CA抑制剂敏感;免疫调节型大多存在肿瘤相关淋巴细胞浸润(TIL)和免疫相关分子的表达,可能对免疫治疗,如PD-1/PD-L1抑制剂、肿瘤疫苗等表现出更为敏感的特性。已有证据表明不同的TNBC亚型对含蒽环、紫杉类药物的新辅助化疗方案反应不同,BL1肿瘤有最高的病理完全缓解率(pCR)为52%,而BL2、LAR、MSL的pCR率分别为0、10%和23%【2】。 随着二代测序技术的发展,对TNBC的分子改变也有进一步的研究。每位TNBC患者平均携带约60个体细胞突变,个体间的突变负荷存在差异。TP53被认为是TNBC中最常见的突变基因,突变率为60%~70%;其次为PIK3CA基因突变,约为10%,在AR亚型中该基因的突变更为常见约46.2%。其他基因在TNBC中的突变频率为1%~5%,但这些低频突变却很可能是致命性的驱动突变或一些可治疗性的突变,因而靶向这些关键性的驱动突变的治疗可能为TNBC未来的精准治疗带来曙光。 2 TNBC精准治疗机遇 目前,TNBC治疗手段仍以化疗为主,而精准检测技术的革新,使得对TNBC认识更为深入,不同亚型有其独特的生物学特征。此外,基因测序的结果显示出TNBC更高的肿瘤突变负荷,这些都为靶向这类疾病的治疗提供可能的理论依据。近年来,一些新的治疗手段不断问世,给TNBC的治疗带来新的机遇。 2.1 BRCA1/2突变 在20世纪90年代初,首次发现某个基因与乳腺癌的发生密切相关,命名为BRCA基因,该基因在体内主要起到识别DNA损失和触发细胞凋亡的作用。在乳腺癌中,BRCA1/2胚系突变是基底样型乳腺癌的特征之一,在TNBC中检出率约为10%,但BRCA1/2胚系突变并非只能发生在TNBC中。 BRCA1突变细胞对铂类药物有较高的敏感性。在新辅助化疗阶段,国内数据显示仅蒽环联合紫杉类药物治疗TNBC的pCR率高达40%以上【3】。对于BRCA1/2突变患者,研究表明铂类单药的pCR率高达61%~90%【4】,显著高于蒽环联合紫杉类新辅助化疗方案在TNBC人群中的pCR率。在晚期BRCA1/2突变乳腺癌中,铂类药物同样显示出良好的活性。TB-CRC009【5】结果显示,与整体人群相比,铂类单药对BRCA1/2胚系突变的患者具有更好的活性。TNT【6】是一项对比卡铂与多西他赛在TNBC或BRCA1/2突变晚期乳腺癌患者中的有效性研究,结果表明虽然两个方案在整体人群中的有效率、PFS及OS相似,但卡铂对BRCA1/2突变携带者更有效。 除了铂类药物,PARP抑制剂可能是BRCA1/2突变未来治疗方向之一。聚二磷酸腺苷聚合酶(PARP)是一种参与碱基剔除修复的关键酶,在BRCA1/2突变的细胞中,同源修复(HR)如无PARP酶参与,将导致细胞周期阻滞及凋亡。有报道显示,在BRCA1/2突变的转移性乳腺癌中单药PARP抑制剂奥拉帕利(olaparib)的客观缓解率为12.9%~41.0%【7-8】。在联合治疗方面,奥拉帕利联合顺铂对于BRCA1/2突变的晚期乳腺癌患者的有效率高达71%【9】,均高于顺铂和奥拉帕利单药的有效率。虽然在乳腺癌中奥拉帕利有一定疗效,但另一PARP抑制剂依尼帕利(iniparib)的临床结果并未达到预期目标,其Ⅲ期临床试验结果为阴性【10】,原因可能是TNBC异质性较大,PAPR抑制剂并非对所有TNBC有效,因而奥拉帕利针对BRCA1/2突变的TNBCⅢ期临床试验将在乳腺癌中验证PARP抑制剂的疗效。 临床实践中,因BRCA1/2突变的晚期乳腺癌患者对铂类药物有较高的反应率和更长的获益时间,建议首选含铂类的治疗方案。对于早期乳腺癌,目前的标准仍然是含蒽环、紫杉类药物方案,针对铂类药物可能获益的患者,标准方案联合铂类药物可进一步提高治愈率,但需注意的是联合铂类药物的毒性管理(如卡铂的骨髓毒性)【11】。从机制上看,PARP抑制剂未来将成为BRCA1/2突变患者的标准治疗,但目前证据并不充分。 2.2 PIK3CA信号通路 PIK3CA基因在TNBC中突变率约为10%,最常见突变区域为编码PI3K蛋白的α亚基区域,PI3K通路的负性调节因子PTEN缺失在TNBC中的发生率约为9.6%【12】,因此靶向PI3K通路可能是部分TNBC精准治疗的方向。研究表明,在非AR亚型中联合PI3K抑制剂和PARP抑制剂不仅能调节细胞增殖、存活和凋亡,而且能增强BRCA1/2突变的TNBC对PARP抑制剂的敏感性【13】。因此,一项PI3K抑制剂布帕利西(buparlisib)联合奥拉帕利的临床Ⅰ期试验目前正在包括晚期TNBC的实体瘤中进行【14】。 2.3 VEGF信号通路 血管内皮生长因子(VEGF)信号通路在TNBC中起到关键性的抑制血管生成作用。贝伐珠单抗是目前唯一被批准用于治疗乳腺癌的抗血管生成药物。研究表明,贝伐珠单抗联合紫杉类药物或卡培他滨显著改善TNBC患者的PFS【15-17】。此外,一些小分子酪氨酸激酶抑制剂(TKI)通过结合VEGF受体胞内区域抑制血管生成,阿帕替尼即是一类高选择竞争性结合VEGF受体-2胞内ATP结合位点药物,与其他小分子TKI相比具有更高的抑制血管生成活性。在二线治疗后的晚期胃癌患者中,阿帕替尼显示出较好的安全性和有效性【18】。在转移性TNBC中,阿帕替尼单药同样显示出较好的安全性和有效性【19】。因此,抗血管生成抑制剂策略也是TNBC精准治疗的机遇。 2.4 AR受体通路 体内外的研究表明,TNBC中的AR亚型显示出对AR抑制剂有较好的反应性【1】。在AR阳性晚期TNBC中一项临床Ⅱ期试验评估了AR抑制剂比卡鲁胺(bicalutamide)的有效性和安全性,采用免疫组织化学法检测AR核染色>10%定义为AR阳性,接受单药比卡鲁胺治疗6个月的随访结果显示临床获益率为19%,中位PFS为12周【20】,是一项首次AR阳性TNBC患者的内分泌治疗研究。随后,一项临床Ⅱ期试验评估了另一AR抑制剂恩杂鲁胺(enzalutamide)在晚期AR阳性TNBC中的疗效,入组75例AR阳性TNBC患者,其客观有效率为35%,平均PFS为14.7周,通过基因表达谱能检测一种雄激素驱动基因(Dx)预测更高的临床获益,可能是未来精准抗AR受体治疗的研究方向【21】。同时细胞系研究中的AR受体亚型的TNBC富含PIK3CA活化突变,对AR抑制剂和PIK3CA抑制剂双重敏感,恩杂鲁胺联合PI3K抑制剂他塞利西(taselisib)治疗AR阳性TNBC患者的Ⅰ/Ⅱ期临床试验正在进行中。 尽管理论上靶向AR的内分泌治疗前景广阔,但要作为常规临床实践仍需要更高级别循证医学证据。未来该领域亟待解决的问题是寻找预测抗AR抑制剂疗效的生物学标志物以指导临床实践。 2.5 免疫检查点抑制剂 由于基因组不稳定性和肿瘤突变负荷导致TNBC有较强的抗原性,另外TNBC中的TIL【22】、PD-L1【23】和mRNA【24】表达均较其他乳腺癌亚型高。因此,免疫治疗被认为是TNBC一个重要的治疗手段。 近期报道显示免疫检查点抑制剂在TNBC中具有良好活性,在Ⅰ期临床试验中27例PD-L1表达阳性的TNBC患者接受PD-1单克隆抗体培布罗珠单抗(pembrolizumab)单药治疗后客观有效率为18.5%,平均PFS为17.9周,另有7例患者疾病达到稳定【25】。另一项Ⅰ期临床试验表明,21例可评价的PD-L1阳性TNBC患者接受PD-L1单克隆抗体阿特珠单抗(atezolizumab)治疗后客观有效率为33%,所有患者均在6周内可评价疗效【26】。正在进行中的GP28328研究对24例晚期TNBC患者行白蛋白结合型紫杉醇联合阿特珠单抗治疗后,一线解救治疗的客观缓解率为46%,二、三线治疗的客观有效率分别为22%和40%。 上述研究证明免疫治疗对多线治疗后的晚期TNBC患者疗效可观。目前全球正在进行的免疫检查点抑制剂的研究将逐渐解决有关最佳的免疫治疗适宜人群、预测疗效的生物标志物的筛选,以及最佳的用药顺序等问题,相信将为TNBC患者带来更加获益的精准免疫治疗。 3 结语 与其他亚型的乳腺癌相比,虽TNBC整体预后较差,更易发生内脏及中枢神经系统转移,但精准医疗模式的发展将为提高TNBC预后提供机遇。通过高通量测序技术和基因组学技术将进一步对TNBC某些基因驱动的疾病进行细分,靶向这些基因实现TN-BC患者精准治疗,如BRCA1/2突变给予铂类药物和PARP抑制剂、AR受体阳性给予AR拮抗剂、PD-1/PD-L1阳性给予免疫检查点抑制剂的治疗。未来在精准全程管理理念的指导下,化疗、内分泌、靶向、免疫治疗将可能成为TNBC患者的标准治疗模式。参考文献Lehmann BD, Bauer JA, Chen X, et al. Identification of human triplenegative breast cancer subtypes and preclinical models for selection of targeted therapies. J Clin Invest. 2011;121(7):2750-2767.Masuda H, Baggerly KA, Wang Y, et al. Differential response to neoadjuvant chemotherapy among 7 triple-negative breast cancer molecular subtypes. Clin Cancer Res. 2013;19(19):5533-5540.刘伟, 李健斌, 王涛, 等. 蒽环类联合紫杉类方案在乳腺癌新辅助化疗中的有效性及安全性评价. 临床肿瘤学杂志. 2016;21(3):228-232.Byrski T, Huzarski T, Dent R, et al. Pathologic complete response to neoadjuvant cisplatin in BRCA1-positive breast cancer patients. Breast Cancer Res Treat. 2014;147(2):401-405.Isakoff SJ, Mayer EL, He L, et al. TBCRC009: a multicenter phase II clinical trial of platinum monotherapy with biomarker assessment in metastatic triple-negative breast cancer. J Clin Oncol. 2015;33(17):1902-1909.Gerratana L, Fanotto V, Pelizzari G, et al. Do platinum salts fit all triple negative breast cancers? Cancer Treat Rev. 2016;48:34-41.Kaufman B, Shapira-Frommer R, Schmutzler RK, et al. Olaparib monotherapy in patients with advanced cancer and a germline BRCA1/2 mutation. J Clin Oncol. 2015;33(3):244-250.Sonnenblick A, de Azambuja E, Azim HA Jr, et al. An update on PARP inhibitors-moving to the adjuvant setting. Nat Rev Clin Oncol. 2015;12(1):27-41.Balmana J, Tung NM, Isakoff SJ, et al. Phase I trial of olaparib in combination with cisplatin for the treatment of patients with advanced breast, ovarian and other solid tumors. Ann Oncol. 2014;25(8):1656-1663.O'Shaughnessy J, Schwartzberg L, Danso MA, et al. Phase III study of iniparib plus gemcitabine and carboplatin versus gemcitabine and carboplatin in patients with metastatic triple-negative breast cancer. J Clin Oncol. 2014;32(34):3840-3847.江泽飞. 乳腺癌治疗决策:从个体化治疗到精准医学. 中国实用外科杂志. 2015;35(7):697-700.Shah SP, Roth A, Goya R, et al. The clonal and mutational evolution spectrum of primary triple-negative breast cancers. Nature. 2012;486(7403):395-399.Ibrahim YH, García-García C, Serra V, et al. PI3K inhibition impairs BRCA1/2 expression and sensitizes BRCA-proficient triple-negative breast cancer to PARP inhibition. Cancer Discov. 2012;2(11):1036-1047.Miller K, Wang M, Gralow J, et al. Paclitaxel plus bevacizumab versus paclitaxel alone for metastatic breast cancer. N Engl J Med. 2007;357(26):2666-2676.Hosoya N, Miyagawa K. Targeting DNA damage response in cancer therapy. Cancer Sci. 2014;105(4):370-388.Robert NJ, Diéras V, Glaspy J, et al. RIBBON-1: randomized, doubleblind, placebo-controlled, phase III trial of chemotherapy with or without bevacizumab for first-line treatment of human epidermal growth factor receptor 2-negative, locally recurrent or metastatic breast cancer. J Clin Oncol. 2011;29(10):1252-1260.Brufsky AM, Hurvitz S, Perez E, et al. RIBBON-2: a randomized, double-blind, placebo-controlled, phase III trial evaluating the efficacy and safety of bevacizumab in combination with chemotherapy for second-line treatment of human epidermal growth factor receptor 2-negative metastatic breast cancer. J Clin Oncol. 2011;29(32):4286-4293.Li J, Qin S, Xu J, et al. Apatinib for chemotherapy-refractory advanced metastatic gastric cancer: results from a randomized, placebo-controlled, parallel-arm, phase II trial. J Clin Oncol. 2013;31(26):3219-3225.Hu X, Zhang J, Xu B, et al. Multicenter phaseII study of apatinib, a novel VEGFR inhibitor in heavily pretreated patients with metastatic triple-negative breast cancer. Int J Cancer. 2014;135(8):1961-1969.Gucalp A, Tolaney S, Isakoff SJ, et al. Phase II trial of bicalutamide in patients with androgen receptor-positive, estrogen receptornegative metastatic breast cancer. Clin Cancer Res. 2013;19(19):5505-5512.廖宁. 2015年乳腺癌研究进展. 循证医学. 2016;16(1):9-14.Loi S, Sirtaine N, Piette F, et al. Prognostic and predictive value of tumor-infiltrating lymphocytes in a phase III randomized adjuvant breast cancer trial in node-positive breast cancer comparing the addition of docetaxel to doxorubicin with doxorubicin-based chemotherapy: BIG 02-98. J Clin Oncol. 2013;31(7):860-867.Ali HR, Glont SE, Blows FM, et al. PD-L1 protein expression in breast cancer is rare, enriched in basal-like tumours and associated with infiltrating lymphocytes. Ann Oncol. 2015;26(7):1488-1493.Sabatier R, Finetti P, Mamessier E, et al. Prognostic and predictive value of PDL1 expression in breast cancer. Oncotarget. 2015;6(7):5449-5464.Nanada R, Chow LQ, Dees EC, et al. Pembrolizumab in patients with advanced triple-negative breast cancer: phase Ib KEYNOTE-012 study. J Clin Oncol. 2016;34(21):2460-2467.Gibson J. Anti-PD-L1 for metastatic triple-negative breast cancer. Lancet Oncol. 2015;16(6):e264.原文参见:中国肿瘤临床. 2016;43(24):1074-1077.
刘战丛 主任医师 漯河市中心医院 肝胆胰脾外科554人已读 - 诊后必读 乳腺癌化疗注意事项
一、积极配合医务人员做好化疗的思想准备。漯河市中心医院普通外科刘战丛二、化疗会导致程度不同的恶心,呕吐症状,应正确对待,鼓励自己多进食,以下措施可减轻胃部不适1.护士会遵医嘱及时使用镇静、止吐药物2.保持病室内空气清新,避免引起不适的气味如烟味,香水,消毒剂等气味,室内通风换气3-4次/日3.进食清淡,少油,易消化,富含营养的温热食物,避免进食生冷、辛辣、油炸、油腻、熏腌食物4.少吃多餐,每日进食5-6次,避免食入过饱,以免增加胃部不适。同时应多吃含纤维素丰富的食物保持大便通畅。如土豆,香蕉,绿叶蔬菜等。大便困难者应及时告知医生并对症处理5.尽可能坐起来进餐,半小时后再平卧6.收听喜欢的音乐,收看喜欢的视频节目,有意识分散自己的注意力。三、化疗时应多饮水,保证每日尿量在2000ml以上,有利于保护肾脏功能及化疗后代谢废物排出四,化疗药物会导致骨髓抑制,造成白细胞,血小板等降低而并发感染及出血因此,化疗时及化疗间隙期间应注意下列问题:1.注意保暖,预防感冒,保持口腔清洁,注意尿道口及肛周卫生,以免发生感染2.减少陪伴探视,不到人多的公共场所,以免发生交叉感染3.避免创伤,防止出血4.化疗第8-10天时检查血常规,以便及时给予升白细胞等药物治疗五.化疗后会出现不同程度的脱发现象,在停止治疗后3-6月可重新长出新发,在脱发时,可剃成光头,戴上帽子或假发,保持美观六,化疗间歇期可服用地榆升白片、贞芪扶正颗粒等药物提高免疫力。红枣、香菇、黄芪、山药等有报道有助于提升白细胞,可适量食用七、化疗期间如出现口腔溃疡,可以口服六味地黄丸、知柏地黄丸治疗,复方氯己定含漱液(或复方洗必泰漱口液)漱口八、化疗期间如出现腹泻,多系消化道黏膜损伤所致。可以服用思密达和易蒙停治疗九、化疗期间可以适当进行轻体力活动,但应当注意休息、避免劳累、保证睡眠、保持积极乐观的情绪。不提倡反复研究疾病相关知识而思虑过度。十、化疗期间如出现肩部、颈部出现疼痛及同侧上肢浮肿或疼痛等症状,应及时回医院检查。十一、化疗间歇期应注意下一次化疗的时间,应提前2-3天住院,避免延误。
刘战丛 主任医师 漯河市中心医院 肝胆胰脾外科799人已读 - 医学科普 胆囊结石胆囊炎的患者你还在按冠心病治疗吗?
胆囊炎和冠心病是中老年人中常见和多发的疾病。冠心病发作可引起心绞痛,胆结石和胆囊炎发作也可引起心前区不适。许多病人同时患有这两种疾病,包括胆结石和冠心病。因此,临床上很容易混淆心前区疼痛是由冠状动脉疾病还是胆囊炎引起的。并且胆囊炎也可以诱发冠心病发作,临床上称为胆心综合征。胆心综合征是指胆道系统疾病(胆囊炎、胆结石)等,并通过神经反射引起冠状动脉收缩,导致冠状动脉供血不足(供氧需氧失衡),从而引起心绞痛、心律不齐,甚至心肌梗塞等症状的临床综合症。此类冠心病心脏症状使用硝酸甘油或救心丸不易缓解,用阿托品、杜冷丁则可缓解。多由吃油腻食物或情绪激动而诱发。一、胆系冠心病的发病机制1.血脂异常这是胆石症和冠心病在病因学上相同的诱发因素。血脂尤其是胆固醇的增加是胆石症和动脉粥样硬化形成的基础。其次,肥胖、糖尿病、活动少、吃太多动物脂肪或富含胆固醇的食物是常见的危险因素。2.胆道高压与神经反射心脏受T2~8脊神经支配,而胆囊、胆总管受T4~9脊神经支配,二者在T4~5脊神经处存在交叉。当胆管中的压力增加、胆管痉挛或由胆酸盐刺激产生冲动时,冠状动脉血管通过脊髓-神经节-神经反射被迷走神经间接收缩;冠状动脉血流量、心肌收缩、心搏量和血压的减少会进一步减少冠状动脉血流量并最终导致心肌缺氧,从而诱发心绞痛、心律失常等。这是胆心综合征发病的主要机制。3.胆道感染胆道感染对心肌代谢有严重干扰,主要表现在两个方面,一是感染因素本身的影响,二是肝功能损害造成的间接影响。感染对心肌的损害不仅是细菌毒素的直接作用,也是体温、电解质、循环血容量、内环境酸碱度、渗透压异常和能量代谢紊乱的影响。胆道疾病引起的水和电解质紊乱,尤其是低钾血症是临床心电图改变的常见原因。4.胆绞痛的胆囊炎症刺激可导致各种心血管效应,尤其是存在多年的结石性胆囊炎。炎症和疼痛会反过来导致心率减慢、血压下降和冠状动脉供血减少,从而导致一系列心电图变化。此外,有冠心病基础的老年患者,由于胆道疾病的影响,更有可能患有胆心综合征。二、胆系冠心病临床表现1、心前区疼痛它的性质可能类似于冠心病或心绞痛,但它经常发生在饱餐后,并持续很长时间。硝酸甘油效果差,而解痉药和止痛剂如阿托品和哌替啶通常有效。2、心律失常许多胆道疾病患者因心律失常而感到心悸。窦性心律失常和过早收缩在临床上很常见,偶尔会诱发心房颤动和阵发性室上性心动过速。胆道疾病治愈后,上述心律失常可消失。3.心电图变化除心律失常外,约有1/3的患者可能有非特异性ST段压低和T波压低或倒置。当胆囊炎症持续存在时,具有上述心血管疾病表现且无法用其他原因解释的胆道疾病患者应考虑胆心综合征。三、胆系冠心病治疗胆心综合征常伴有急性胆道疾病发作,通常在缓解后自动消失。因此,主要治疗原发性疾病,胆道疾病的心血管表现通常不需要特殊治疗。对于保守治疗患者,除利胆治疗和选择有效抗生素外,还应选择钙拮抗剂硝苯地平进行治疗。顽固性胆囊炎可考虑行胆囊切除术,胆心综合征患者术后心绞痛基本消失。连接------胆心反射(迷走神经反射)是指胆道手术时由于牵扯胆囊,或探查胆道时所引起的心率减慢、血压下降,严重者可因反射性冠状动脉痉挛导致心肌缺血、心律失常,甚至心跳骤停等现象,已处于休克或低血压状态下的病人更易发生,应采取积极措施(局部神经封闭、静脉辅助用药如哌替啶、阿托品)加以防范。它的发生是建立在完整的反射弧基础上的(胆囊、胆道部位的迷走神经分布密集),即胆囊壁内内脏神经感觉纤维受到刺激,经左侧迷走神经内传入纤维将兴奋传至延髓内副交感低级中枢(迷走神经脊核),释放冲动再经过左侧迷走神经内副交感纤维到达心脏。
刘战丛 主任医师 漯河市中心医院 肝胆胰脾外科892人已读 - 诊后必读 分化型甲状腺癌TSH抑制
分化型甲状腺癌(乳头状癌和滤泡状癌)术后必需进行TSH(促甲状腺激素)抑制治疗,TSH的抑制是通过补充外源性甲状腺素(国内常用左甲状腺素,也称优甲乐)来反馈性抑制脑垂体分泌TSH来实现。高危DTC患者术后TSH抑制到<0.1mU/L时,肿瘤复发,转移显著降低,低危DTC患者术后TSH抑制到0.1~0.5mU/L时即可明显改善总体预后,那些不表达TSH的甲状腺癌,如未分化癌,髓样癌,某些低分化的DTC,即使将TSH抑制到很低的水平也不能抑制肿瘤生长。TSH抑制治疗副作用会造成亚临床甲亢,加重心脏负担和心肌缺血(尤其在老年患者),引发或加重心率紊乱(特别是房颤),导致心血管疾病相关死亡风险增高。TSH抑制的另一副作用是增加绝经后妇女的骨质疏松发生率,严重时会出现病理性骨折。DTC术后复发危险度分为低、中、高危3层。低危组需符合以下全部条件:无局部或远处转移;所有肉眼可见的肿瘤均被清除;肿瘤未侵犯周围组织;肿瘤不是侵袭性的组织学亚型,并且没有血管侵犯;清甲后行全身碘131显像,甲状腺床以外无碘摄取。中危组须符合以下条件之一:初次手术后病理检查可在镜下发现甲状腺周围软组织侵犯;有颈部淋巴结转移;肿瘤是侵袭性的组织学亚型;肿瘤侵犯了血管;清甲后行全身碘131显像,甲状腺床以外有碘摄取。高危组需符合以下条件之一:肉眼下可见肿瘤侵犯周围组织或器官;肿瘤未能完整切除,术中有肿瘤残留;有远处转移;全甲状腺切除后血清甲状腺球蛋白(Tg)水平仍较高;有甲状腺癌家族史。TSH抑制治疗副作用风险同样分为低、中、高危3层。低危组符合下列所有条件:中青年;无症状;无心血管疾病;无心律失常;无肾上腺素能受体激动的症状或体征(怕热、多汗、多食、消瘦、易激动);无心血管疾病危险因素(肥胖、高血压、高血脂、高血糖);无合并疾病;绝经前妇女;骨密度正常;无骨质疏松的危险因素。中危组需满足下列条件之一:中年;高血压;有肾上腺素能受体激动的症状或体征;吸烟;有心血管疾病危险因素(肥胖、高血压、高血脂、高血糖);围绝经期妇女;骨密度减小;有骨质疏松的危险因素。高危组需满足任一一条:临床心脏病患者;老年;绝经后妇女;伴发其他严重疾病。DTC术后TSH抑制治疗期限分为初治期和随访期,初治期为术后1年内,随访期在复发低危组为5~10年,中高危组为终身。基于双风险评估的DTC患者术后TSH抑制治疗目标:①在低复发危险-低副作用风险组(双低组)初治期目标值为0.1~0.5mU/L,随访期为0.5~2.0 mU/L,之后根据甲状腺功能情况而定,如果甲功正常无需治疗,如果甲功低下,可仅进行甲状腺激素替代治疗(口服优甲乐)至甲功正常水平。②在低复发-中高副作用风险组,初治期目标值为0.5~1.0 mU/L,随访期为1.0~2.0 mU/L,之后根据甲功行替代治疗。③在中高复发-低副作用风险组,初治期和随访期均为<0.1 mU/L,初治期最好控制在0.04 mU/L④在中高复发-中高副作用风险组,初治期为<0.1 mU/L,随访期为0.1~0.5 mU/L。TSH抑制治疗的副作用风险为中高危层次者,应个体化抑制TSH至接近目标值的最大耐受程度,予以动态调整,同时预防和治疗心血管病和骨质疏松。
刘战丛 主任医师 漯河市中心医院 肝胆胰脾外科1270人已读





